پروتئین الکتروفورز
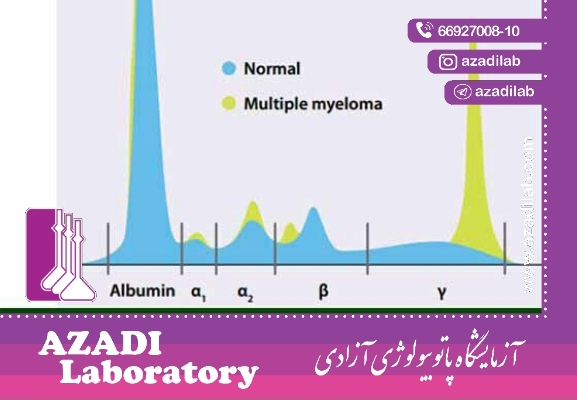
الکتروفورز پروتئین های سرم روشی آسان و ارزان برای جداسازی و بررسی کمی پروتئین های سرم و ادرارمی باشد که بر اساس بار خالص، اندازه و شکل آن ها انجام می شود. سرم حاوی بیش از هزار پروتئین است که هر یک عملکردهای ویژه خود را دارند و غلظت آنها تحت شرایط پاتولوژیک متفاوت، تغییر می کند. پروتئین های سرم بر پایه بار الکتریکی خود به پنج بخش مجزا شامل آلبومین، آلفا ۱- گلوبولین (α۱)، آلفا ۲- گلوبولین (α۲)، بتاگلوبولین (β) و گاماگلوبولین (γ) تفکیک می شوند.
ارزیابی اجزای پروتئین های سرم برای تشخیص، بررسی و کنترل دوره بیماری مبتلایان به سرطان (لنفوم، میلوما)، بیماری های
روده ای- کلیوی همراه با دفع پروتئین، اختلالات کبدی، اختلالات ایمنی، مونوکلونال گاماپاتی ها، میلوم متعدد، ماکروگلوبولینمی والدن اشتروم، سوء تغذیه و بیماری های مزمن همراه با ادم استفاده می گردد.
روند جداسازی پروتئین ها شامل قرار دادن آن ها در یک ماتریکس و سپس مشاهده ی حرکت پروتئین در حضور یک میدان الکتریکی می باشد. پروتئین ها از اتصال کووالان اسید آمینه ها تشکیل شده اند و دارای اندازه و بارهای الکتریکی متفاوتی هستند، بنابراین می توان آنها را از نظر الکتروشیمیایی جدا نمود. پروتئین ها در یک بافر قلیایی (PH=5.8-9) شارژ منفی می گیرند و از الکترود منفی به سمت الکترود مثبت مهاجرت می کنند. ماتریکس الکتروفورز، ژل آگارز است و پروتئین ها بر اساس تراکم بار سطحی خود از یکدیگر جدا می شوند.
پروتئین توتال
پروتئین ها در ساختار عضلات، آنزیم ها، هورمون ها، پروتئین های ناقل و سایر اجزای عملکردی و ساختاری بدن شرکت می کنند. سطح پروتئین های سرم در سوء تغذیه ، بعد از جراحی، بیماران دچار سوختگی، مبتلایان به انتروپاتی و اوروپاتی کاهش می یابد. همچنین در سه ماهه سوم بارداری کاهش میزان پروتئین توتال مشاهده می شود. در بعضی بیماری ها مانند بیماری های مزمن کبدی فقط آلبومین کاهش می یابد و میزان گلبولین ها طبیعی بوده و یا برای حفظ سطح کلی پروتئین تام افزایش یافته اند. در این بیماری ها اگر نسبت آلبومین به گلبولین را اندازه گیری نمایید، این تغییرات قابل شناسایی خواهند بود. به طور معمول این نسبت باید از ۱ بیشتر باشد. در بعضی از بیماری ها نظیر مولتیپل میلوما و گاماپاتی ها افزایش سطح پروتئین توتال روی می دهد. پروتئین توتال سرم ترکیبی از پره آلبومین، آلبومین و گلوبولین ها می باشد. در انجام الکتروفورز پروتئین آلبومین با فاصله بیشتری حرکت نموده است، به دنبال آن تعدادی باند گلوبولینی که به ترتیب β،α۲،α۱ ( معمولا به β۱ و β۲ تجزیه می شود) و نهایتا γ گلوبولین مشخص می شوند.
مقادیر طبیعی: ۸٫۳ –۶٫۴ گرم در دسی لیتر
آلبومین
آلبومین پروتئین اصلی سرم که اغلب دو سوم (۶۰ درصد) پروتئین توتال را تشکیل می دهد، در کبد ساخته می شود. مهمترین عمل آلبومین در خون حفظ فشار اسموتیک کلوئیدی می باشد. همچنین آلبومین حمل کننده داروها، هورمون ها و آنزیم ها در خون می باشد. نیمه عمر آن ۱۸-۱۲ روز است. بلندترین قله (به صورت یک تک باند بلند) و نزدیکترین باند به الکترود مثبت را در الکتروفورز به خود اختصاص می دهد.
آلبومین معیار خوبی برای ارزیابی عملکرد کبد می باشد.
عواملی مانند سوء تغذیه، بارداری، بیماری کبدی (سیروز، هپاتیت و نکروز کبدی)، افزایش حجم خون، عفونت های حاد، سندرم نفروتیک، انتروپاتی های توأم با دفع پروتئین و بیماری های التهابی منجر به کاهش آلبومین می شوند.
کم شدن آب بدن (Dehydration) یکی از دلایل افزایش آلبومین می باشد.
حرکت بیش از حد آلبومین به سمت آند در نتیجه اتصال به بیلی روبین، اسیدهای چرب غیر استریفیه، پنی سیلین و استیل سالیسیلیک اسید و در بعضی مواقع در پانکراتیت حاد روی می دهد.
مقادیر طبیعی: ۵-۳٫۵ گرم در دسی لیتر
گلوبولین ها
گلوبولین ها بخش بسیار کوچکتر از کل پروتئین های سرم را تشکیل می دهند. همان طور که گفته شد پنج طبقه بندی از گلوبولین ها وجود دارد:β۲،β۱،α۲،α۱ و γ که نزدیکترین باند به الکترود منفی، γ است. نقش گلوبولین ها در حفظ فشار اسمزی بسیار کمتر از نقش آلبومین است.
مقادیر طبیعی: ۳٫۴ -۲٫۳ گرم در دسی لیتر
آلفا ۱- گلبولین
آلفا ۱- آنتی تریپسین یک پروتئین واکنشگر حاد است که بیشتر آلفا۱- گلبولین ها را تشکیل می دهد. بعضی از پروتئین های ناقل نظیرگلوبولین پیوندشونده به کورتیکواستروئید (CBG) و گلوبولین متصل به تیروکسین (TBG) نیز دراین ناحیه قرار می گیرند.
آلفا ۱- آنتی تریپسین نوعی پروتئین فاز حاد است که در بیماری هایی که همراه با التهاب، نکروز، انفارکتوس، بدخیمی یا سوختگی افزایش می یابد.
کاهش یا فقدان ژنتیکی آنزیمی آلفا ۱- آنتی تریپسین (آمفیزم ریوی جوانان) موجب کاهش سطح آلفا-۱- گلوبولین
می شود این آنزیم نقش مهمی در عملکرد طبیعی ریه دارد.
پروتئین بنس جونز (Bence Jones Protein) می تواند به α۱ متصل شده و باعث تاخیر در حرکت باند α۱ گردد.